2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
13.1.1 Hypothèse de positivité
13.1.3 Échangeabilité conditionnelle
13.2 Petite introduction à l’inférence causale
13.3 Association n’est pas causalité
13.3.1 DAG générique des comparaisons externes
13.4 Effet causal, estimand causal , cible de l’inférence
13.4.1 Effet traitement moyen (average treatment effect)
13.4.2 Analyse en intention de traiter (as started ) / analyse per protocole (as treated )
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
18 Identifications des patients dans la source de données
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
La mise en évidence directe de l’effet causal d’un facteur donné nécessite de pouvoir comparer l’état d’un système en la présence et en l’absence de ce facteur. L’effet de ce facteur sera donné par la différence entre ces 2 états. Ainsi la détermination d’un effet causal nécessite de pouvoir observer le même système avec et sans le facteur étudié.
Soit Y l’état du système et a le facteur étudié qui a 2 modalités a=0 ou a=1 .
L’effet causal produit par le facteur a sera déduite de :
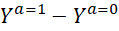
Où 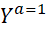 désigne l’état du système quand a=1
et
désigne l’état du système quand a=1
et 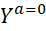 son état quand a=0
.
son état quand a=0
.
Si l’on veut transposer cette formalisation de la causalité aux traitements, Y correspond au critère de jugement (l’outcome) et a au traitement avec a=0 l’absence de traitement et a=1 la prise du traitement.
Pour un patient i , l’effet causal du traitement est donc la différence entre la valeur du critère de jugement quand le patient i est traité et sa valeur quand il n’est pas traité :
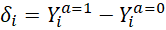
Mais contrairement à beaucoup de systèmes physiques, il va
être impossible d’observer le même patient i
, au même moment de sa
maladie, à la fois avec traitement et sans traitement. Il est donc impossible
d’obtenir la valeur du critère de jugement Y dans ces 2 états, car soit le
patient est traité soit il n’est pas traité. Il est donc impossible d’observer
l’effet du traitement 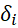 chez un patient.
chez un patient.
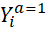 et
et 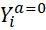 sont appelés outcomes potentiels (potential outcome ),
le terme potentiel signifiant que ces deux valeurs existent potentiellement (ont
une vraie signification) mais qu’ils ne sont pas accessibles toutes les deux
pour le même patient. En effet, soit le patient est traité, soit il n’est pas
traité. Un seul de ces 2 outcomes potentiels est donc observable par les patients
(mais il est facile de convenir que si un patient est traité, le critère de
jugement aurait eu une autre valeur sans traitement et vice versa).
sont appelés outcomes potentiels (potential outcome ),
le terme potentiel signifiant que ces deux valeurs existent potentiellement (ont
une vraie signification) mais qu’ils ne sont pas accessibles toutes les deux
pour le même patient. En effet, soit le patient est traité, soit il n’est pas
traité. Un seul de ces 2 outcomes potentiels est donc observable par les patients
(mais il est facile de convenir que si un patient est traité, le critère de
jugement aurait eu une autre valeur sans traitement et vice versa).
Pour tenir compte de la variabilité inter sujets, l’estimation de l‘effet d’un traitement doit être envisagée au niveau populationnel, statistique. Cela ne change rien à la notion de causalité seulement celle-ci est une causalité stochastique, appréhendable qu’à un niveau populationnel sous la forme d’un effet traitement moyen (ce qui est le cadre classique de l’évaluation des traitements).
Y est alors une variable aléatoire, c’est-à-dire une variable qui est susceptible de prendre une valeur différente pour chaque patient (sans que cela ne soit prévisible d’où l’assimilation à un phénomène aléatoire) mais dont la distribution des valeurs peut parfaitement bien se caractériser au niveau populationnel (par exemple par une moyenne et un écart type pour une variable aléatoire distribué normalement).
Ainsi l’effet traitement moyen (average treatment effect , ATE) sera alors
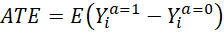
Où 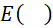 désigne l’espérance mathématique (la
moyenne pour une variable continue ou la fréquence pour une variable binaire).
Ainsi l’effet traitement moyen populationnel sera la moyenne de la différence
des outcome potentiel de chaque patient avec et sans traitement.
désigne l’espérance mathématique (la
moyenne pour une variable continue ou la fréquence pour une variable binaire).
Ainsi l’effet traitement moyen populationnel sera la moyenne de la différence
des outcome potentiel de chaque patient avec et sans traitement.
Mais cette valeur est inaccessible, car les outcomes
potentiels ne sont pas tous les 2 mesurables simultanément chez un même
patient. Une seule mesure est possible par patient, Y
, qui est soit la
valeur de l’outcome avec le traitement a=1
soit sans le traitement a=0
.
Le tableau (ci-dessous) illustre la différence entre l’outcome mesuré et les
outcomes potentiels dans une situation hypothétique où l’on pourrait connaitre
les valeurs des 2 outcomes potentiels de 5 patients. T i
désigne le traitement réellement appliqué au patient i
et Y i
la valeur de son critère de jugement. Quand le traitement du patient est T=1
, Y
prend la valeur de l’outcome potentiel avec traitement 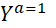 et quand T=0,
Y
est égal à
l’outcome potentiel sans traitement.
et quand T=0,
Y
est égal à
l’outcome potentiel sans traitement.
|
|
|
|
|
Patient 1 |
210 |
220 |
220 |
0 |
Patient 2 |
168 |
178 |
168 |
1 |
Patient 3 |
196 |
205 |
196 |
1 |
Patient 4 |
187 |
197 |
197 |
0 |
Patient 5 |
182 |
190 |
190 |
0 |
En pratique on peut donc mesure avec une série de patients traités ou non traités
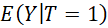 et
et 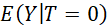 , c’est-à-dire la moyenne des valeurs de
l’outcome Y
chez des patients traités (T=1) (la notation
, c’est-à-dire la moyenne des valeurs de
l’outcome Y
chez des patients traités (T=1) (la notation 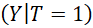 signifie valeurs de la variable Y
quand la variable T
est égale à 1).
signifie valeurs de la variable Y
quand la variable T
est égale à 1).
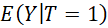 et
et 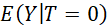 sont donc les moyennes des valeurs de
deux groupes de patients l’un traité et l’autre non traité. La comparaison de
ces 2 valeurs est de l’ordre de la recherche de l’association statistique, mais
pas de la causalité var ne correspond pas à l’expression de l’effet causal, car
E(𝑌 │ 𝑇 =1) n’est pas
forcément égale à
sont donc les moyennes des valeurs de
deux groupes de patients l’un traité et l’autre non traité. La comparaison de
ces 2 valeurs est de l’ordre de la recherche de l’association statistique, mais
pas de la causalité var ne correspond pas à l’expression de l’effet causal, car
E(𝑌 │ 𝑇 =1) n’est pas
forcément égale à 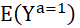 et
et 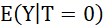 à
à 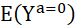 .
.
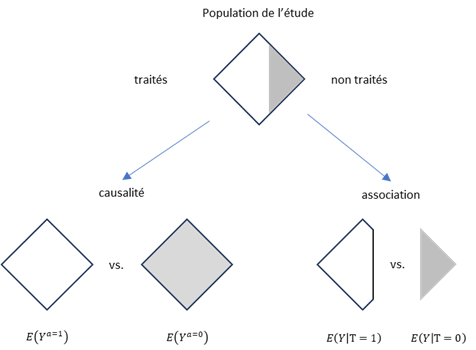
Figure 3 – Représentation graphique de la différence entre association et causalité (reproduit de réf. [112] ).
Ainsi on se retrouve dans une situation où l’on peut
seulement, à partir des données d’une étude, connaitre 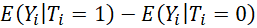 alors qu’il faudrait pouvoir connaitre
alors qu’il faudrait pouvoir connaitre 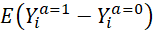 pour pouvoir conclure à la causalité. Il
est possible de passer de la première expression à la dernière en faisant un
certain nombre d’hypothèses. Il est ainsi possible de montrer que l’association
statistique a valeur d’effet causal quand ces hypothèses sont vérifiées.
pour pouvoir conclure à la causalité. Il
est possible de passer de la première expression à la dernière en faisant un
certain nombre d’hypothèses. Il est ainsi possible de montrer que l’association
statistique a valeur d’effet causal quand ces hypothèses sont vérifiées.
L’association statistique observée correspond à
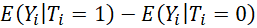
Qui peut être réécrite en faisant l’hypothèse de positivité (1 ci-dessous) et l’hypothèse de cohérence (consistency ) (2 ci-dessous)
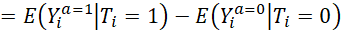
En faisant l’hypothèse d’échangeabilité (3 ci-dessous), cette expression peut se réécrire
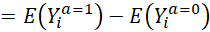
Et comme l’opérateur 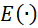 est un opérateur linéaire
est un opérateur linéaire
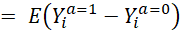
qui est la définition dans le cadre des outcome potentiels de l’effet causal ∎
(1) Si l’hypothèse de positivité est vérifiée alors 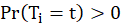 , cela garanti que
, cela garanti que 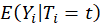 est identifiable dans les deux groupes, sans positivité un
de ces termes conditionnels peut ne pas exister. La quantité
est identifiable dans les deux groupes, sans positivité un
de ces termes conditionnels peut ne pas exister. La quantité 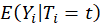 n’est définie que si
n’est définie que si 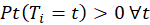 . La positivité assure que le contrefait d’un traitement sera
identifiable (si aucun patient n’a reçu un traitement, on ne peut donc pas
apprendre quoi que ce soit sur leur outcome potentielle sous traitement, même
par extrapolation).
. La positivité assure que le contrefait d’un traitement sera
identifiable (si aucun patient n’a reçu un traitement, on ne peut donc pas
apprendre quoi que ce soit sur leur outcome potentielle sous traitement, même
par extrapolation).
(2) Si l’hypothèse de « Stable Unit Treatment Value
Assumption (SUTVA)” est vérifiée alors 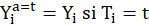
Cela nécessite deux conditions :
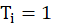 signifie la même chose pour toutes les unités statistiques
signifie la même chose pour toutes les unités statistiques(3) Si l’hypothèse d’échangeabilité est vérifiée, les outcomes potentiels des patients sont les mêmes qu’ils aient reçus un traitement ou l’autre :
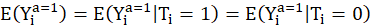
et
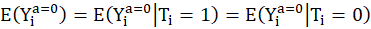
Cependant si les traitements sont donnés en fonction du pronostic des patients :
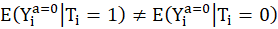
(Des patients de pronostic de base différents ne peuvent pas avoir la même valeur de l’outcome potentiel sans traitement vu que cet outcome potentiel sans traitement correspond au pronostic de base).
L’effet traitement identifié en inférence causale est un effet moyen sur une population (espérance mathématique = moyenne des « effets individuels » de chaque patients i . Cet effet moyen (average treatment effect ) dépend donc de la population cible de l’inférence causale. Cette propriété conduit à la définition de différents effets traitements (ATE, ATT, etc.) (cf. section 13.4)
La meilleure façon s’assurer le respect des hypothèses de l’inférence causale est de réaliser un essai randomisé. La randomisation (comme toute autre méthode de fixation vraiment arbitraire du traitement) assure la positivité et l’échangeabilité. L’hypothèse de cohérence est assurée par la réalisation en double aveugle et en ITT de l’essai.