2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
13.1.1 Hypothèse de positivité
13.1.3 Échangeabilité conditionnelle
13.2 Petite introduction à l’inférence causale
13.3 Association n’est pas causalité
13.3.1 DAG générique des comparaisons externes
13.4 Effet causal, estimand causal , cible de l’inférence
13.4.1 Effet traitement moyen (average treatment effect)
13.4.2 Analyse en intention de traiter (as started ) / analyse per protocole (as treated )
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
18 Identifications des patients dans la source de données
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
L’hypothèse de positivité (positivity assumption ) implique que chaque patient avait une probabilité non nulle (strictement positive) de recevoir l’un ou l’autre des traitements comparés. C’est-à-dire, qu’aucun patient n’avait une impossibilité structurelle de recevoir l’un des 2 traitements.
Cette problématique survient, par exemple, en cas de contre-indications d’un des deux traitements qui ne sont pas des contre-indications de l’autre.
Cela signifie qu’il n’existe aucune caractéristique des patients (ou combinaison de caractéristiques) qui empêchent de recevoir l’un des deux traitements comparés (comme des patients ayant une contre-indication formelle à l’un des traitements, mais pas à l’autre). En d’autres termes, à caractéristiques identiques, il doit y avoir une diversité dans les traitements donnés par les médecins dans la vraie vie.
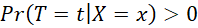
Habituellement cette hypothèse est explorée en comparant les distributions des caractéristiques entre les 2 groupes. Lorsqu’un score de propension est utilisé, l’hypothèse de positivité sera vérifiée lorsque les distributions des scores de propension des deux groupes se chevauchent (cf. section 15.2.3).
On parle aussi d’hypothèse de positivité conditionnelle (conditional positivity )
En cas de non-respect de l’hypothèse de positivité, les estimations seront instables, exposée aux biais et les résultats difficilement généralisables à une population plus large.
Dans les comparaisons externes, plusieurs scénarios peuvent conduire à une rupture (partielle) de l’hypothèse de positivité.
Une de ces situations est constituée par un traitement standard ciblé sur un biomarqueur (et qui n’est utilisé que chez les patients biomarqueurs positifs) et un nouveau traitement qui n’a pas cette restriction. Le nouveau traitement a été évalué dans une étude monobras incluant donc des patients biomarqueurs positifs et négatifs. Le groupe contrôle externe sera constitué uniquement de patients biomarqueurs positifs bien évidemment. Les patients biomarqueurs négatifs présents dans le groupe du nouveau traitement ont une probabilité nulle de recevoir le traitement standard et il y a rupture de la positivité. Ce non-respect de la positivité ne peut pas être solutionné par restriction de population du nouveau traitement au biomarqueur positif, car ce biomarqueur n’a pas été mesuré dans l’étude monobras (pour laquelle il était inutile). Ce point illustre l’importance de concevoir la comparaison externe au moment de la conception de l’étude monobras. Dans ce cas cela aurait permis de percevoir l’importance de mesurer ce biomarqueur dans cette étude même s’il est sans utilité pour le nouveau traitement.
Cette situation pourrait avoir une solution à la condition qu’il soit parfaitement bien démontré que le biomarqueur n’est pas un facteur pronostique, démonstration difficile à produire et qui en général n’est pas disponible. Cette condition rajoute une hypothèse forte, souvent intestable, limitant davantage cette approche pour les comparaisons de ce type.
Si malgré tout c’est le cas, et que le résultat de cette comparaison externe est acceptable, cette comparaison externe ne documentera que le bénéfice du nouveau traitement chez les patients biomarqueurs positifs, car ce n’est qu’uniquement chez ces patients que la comparaison versus traitement ce traitement standard à un sens médical. Donc dans une population différente de l’indication recherchée par le nouveau traitement. À ce niveau se pose aussi la question du choix de l’estimand, ATC (average treatment effect among control ) correspondant plus à la question posée que l’ATT (average treatment effect among treated ) qui est pourtant l’estimand logique des comparaisons à un groupe externe en dehors de cette situation.
Comme le nouveau traitement s’adresse aussi aux patients biomarqueurs négatifs, il va être aussi nécessaire de réaliser une autre comparaison externe versus le traitement standard actuel de ces patients. La même problématique de non-vérification de l’hypothèse de positivité se posera.
Une autre situation de non-vérification (partielle) de l’hypothèse de positivité sera la situation en miroir avec un nouveau traitement ciblé et un traitement standard non ciblé.