2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
17.1 Déplétion des susceptibles
17.2 Biais lié à un défaut de synchronisation des t0
17.3 Groupe contrôle externe non-traité
17.5 Le biais de sélection vu en termes statistiques : censure à gauche, censure à droite
18 Identifications des patients dans la source de données
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
Un groupe contrôle où des patients traités de longue date seraient inclus sans que le suivi disponible enregistré dans la source de données remonte jusqu’à l’initiation de leur traitement peut induire un biais de sélection par déplétion des susceptibles (outcome susceptible ). On parle dans ce cas de patients prévalents car le traitement est déjà instauré quand le patient commence à être suivi par l’étude. La définition de la baseline n’est donc la même pour les patients incidents et les patients prévalent.
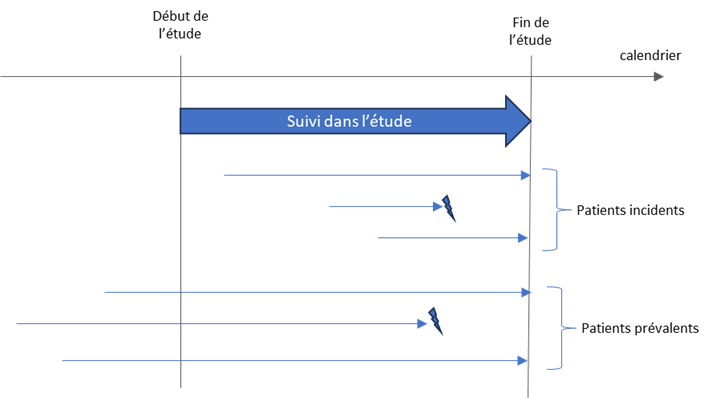
Figure 13 – Définition des patients prévalents et incidents Le début des flèches représente l’initiation du traitement. Seuls les événements survenant durant le suivi dans l'étude seront enregistrés.
Par exemple, il pourrait apparaitre que le nouveau traitement induit plus d’effets indésirables que le traitement contrôle sans que cela soit vraiment le cas en réalité.
Avec des anticoagulants, par exemple, il pourrait faussement apparaitre que le nouveau traitement est plus pourvoyeur d’hémorragies que le contrôle. En effet, dans une étude monobras, le traitement des patients avec le nouveau traitement est initié dans l’étude. Les sujets sont donc suivis depuis l’initiation du traitement. On parle de patients incidents. Tout effet indésirable (toute hémorragie) survenant précocement chez ces patients est observé durant le suivi dans l’étude et colligé.
En revanche, dans un groupe contrôle de patients prévalents, le suivi ne débute pas à l’initiation du traitement, mais alors que les patients prennent déjà le traitement depuis un certain temps. Il se peut alors que des patients ayant initiés dans le passé le traitement contrôle aient présenté avec la même fréquence les mêmes effets indésirables (hémorragies) que les patients recevant le nouveau traitement. Cependant, la survenue de l’effet indésirable ayant mis fin au traitement, ces patients ne seront pas inclus dans le groupe contrôle car non traité au moment où le groupe contrôle sélectionne ses patients dans la source de données (fenêtre de sélection note n° 21 ). Ainsi en prenant des patients déjà traités, il y aura déplétion des patients susceptibles de faire un effet indésirable.
Ainsi ce phénomène de déplétion des susceptibles répond bien à la définition générale du biais de sélection (cf. supra) car l’exclusion de l’étude des patients susceptibles de faire l’événement dépend bien du traitement (elle n’a lieu que dans le groupe contrôle est constitué de patients avec un traitement prévalent) et de la survenue du critère de jugement. On peut expliquer ce biais en disant qu’il y a sélection de patients non susceptible de faire l’événement critère de jugement ne survient que dans le groupe contrôle et que cette sélection dépend du critère de jugement, mais de façon passive, indirecte, car ne sont considérés pour l’inclusion dans le groupe contrôle que des patients qui ont pu poursuivre sans encombre un traitement initié précédemment.
Pour éviter cela, le groupe contrôle ne doit être constitué que de patients initiant le traitement contrôle. Dans ce cas leur suivi débutera bien dès l’initiation du traitement et les effets indésirables précoces seront captés de la même manière qu’ils seraient captés dans une étude monobras. On parle de new users design [182] [183] [184] . Cette approche permet de raisonner sur une « inception cohort » où tous les participants sont recrutés à un point de départ commun dans l'évolution de leur pathologie, typiquement le tout début de la maladie ou de l'exposition étudiée. Ils sont ensuite suivis à partir de ce point zéro commun à tous les patients.
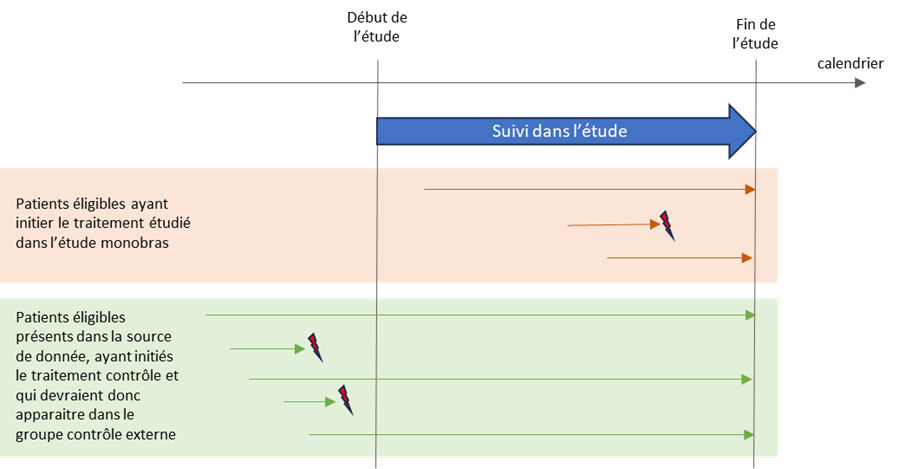
Figure 14 – Mécanisme du biais de sélection par déplétion des susceptibles. Aucun événement n’est observé durant le suivi de l’étude dans le groupe contrôle composé de patients prévalant, car les patients traités avec le traitement contrôle et qui « devait » présenter l’événement l’on fait précocement, avant le début du suivi dans l’étude. Donc, parmi les patients ayant initier le traitement contrôle, seuls arrivent dans l’étude ceux qui « n’ont pas de susceptibilité » à faire l’événement. Il y a eu déplétion des susceptibles dans le groupe des patients ayant initiés le traitement contrôle avant que le suivi de ce groupe dans l’étude débute.
[21] Dans un groupe contrôle externe acceptant des patients prévalents, les patients du groupe contrôle sont sélectionnés dans la source de données à partir du moment où ils reçoivent le traitement contrôle durant la fenêtre temporelle d’inclusion. Seuls des patients ayant débuté le traitement et ne l’ayant pas arrêté précocement pour effet indésirable arriveront toujours traités dans la fenêtre temporelle/calendaire d’inclusion.