2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
17.1 Déplétion des susceptibles
17.2 Biais lié à un défaut de synchronisation des t0
17.3 Groupe contrôle externe non-traité
17.4 Fin du suivi
17.5 Le biais de sélection vu en termes statistiques : censure à gauche, censure à droite
18 Identifications des patients dans la source de données
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
La définition de la fin du suivi peut aussi entrainer un biais de sélection en excluant des périodes de suivi en fin de suivi en fonction du critère de jugement. Il s’agira de censures informatives du suivi liées par exemple à un changement de traitement. Comme le changement de traitement (comme l’arrêt du traitement initial) est potentiellement lié à une évolution de la maladie, censurer le suivi à cet instant introduit une censure informative. Si le groupe traité est suivi jusqu’à une date de point indépendamment des arrêts de traitement, cette asymétrie dans l’estimand utilisé introduira un biais de sélection. La prévention de ce biais nécessite que l’alignement de l’estimand de prise en compte des événements intercurrents entre les deux groupes. Là aussi l’émulation d’un essai cible permet d’éviter des erreurs de design ou d’analyse (cf. section 22). Si le groupe traité utilise l’estimand « policy treatment », avec un suivi systématique et un décompte de tous les événements jusqu’à une date de point arbitraire, un suivi du même type doit être réalisé dans le groupe contrôle.
Dans les groupes traités utilisés dans les comparaisons externes (études monobras ou bras traités d’un essai randomisé) la fin du suivi longitudinal des patients peut être définie principalement de 2 façons. Le suivi s’interrompt simultanément pour tous les patients à la même date calendaire, la date de point (data cut-off) ou le suivi est fixe et identique pour tous les patients, par exemple 52 semaines.
Dans les sources de données, la notion de fin de suivi n’existe pas (dans la quasi-majorité des cas, sauf s’il s’agit par exemple d’un précédent essai randomisé ou d’une précédente monobras). Dans ce cas plusieurs options se présentent.
Une première option est de prendre en compte la totalité du suivi disponible pour les patients sélectionnés pour le groupe contrôle externe. Cela conduira à des courbes de survie tracées sur un temps plus long pour le groupe contrôle que pour le groupe traité (cf. Figure 16).
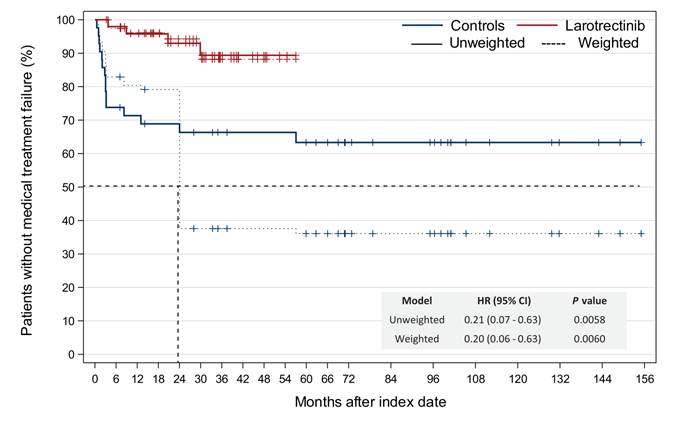
Figure 16 – Exemple de durée de suivi asymétrique entre le groupe traité et le groupe contrôle [193]
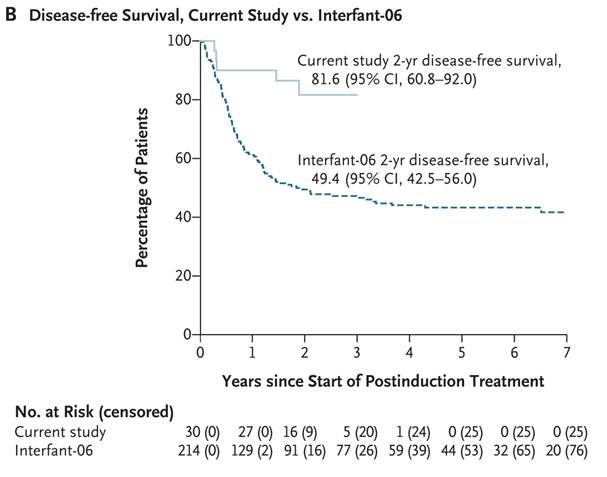
Figure 17 from ref [194]
Parfois le suivi dans le groupe contrôle pourra être inférieur à celui du groupe traité. Cela survient dans les domaines à renouvellement rapide des standards de soins (SOC) comme l’oncologie par exemple. Le SOC actuel auquel veut se comparer le nouveau produit peut être récent, quelques mois par exemple. De plus la source de données peut avoir un délai d’actualisation et ne pas contenir par exemple la dernière année écoulée. La conjonction de ces 2 points peut conduire à un suivi très court pour les patients et leur information disponibles pour le groupe contrôle externe, inférieur à celui de l’étude monobras.
Pour éviter cette différence de suivi entre les deux groupes, il peut être procédé à une troncature des suivis dans le groupe contrôle, en utilisant, par exemple, le suivi maximal du groupe traité. Dans ce cas la distribution des censures liées à la fin du suivi (censures liées à la date de point aussi appelée censures administratives) ne sera pas comparable entre les deux groupes. Dans le groupe traité, ces censures seront étalées dans le temps sur la fin des courbes compte tenu de l’étalement des inclusions dans l’étude d’origine. Dans le groupe contrôle externe, l’étalement de cette censure dépendra uniquement de la position du délai de troncature par rapport à la distribution des suivis disponible dans la source de données. Il est alors possible que tous les patients du groupe contrôle aient la même durée de suivi si le délai de troncature utilisé est inférieur au suivi le plus court disponible dans la source de donnée (et donc il n’existera pas d’étalement des censures de fin de suivi en fin de courbe). Quoi qu’il en soit cette asymétrie de distribution des censures ne pose pas de problème en terme statistique (en termes d’inférence) car ces censures sont non informatives.
Dans le dossier FDA d’évaluation de eflornithine dans les neuroblastomes pédiatriques à haut risque [195] , il existe une grande asymétrie des durées de suivi entre l’étude monobras de l’eflornithine et le groupe control externe.
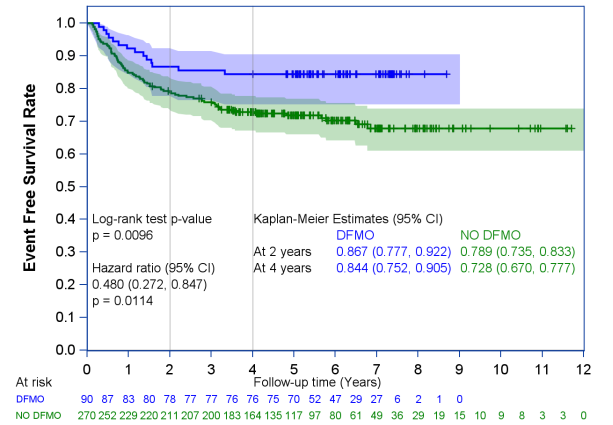
Des analyse de sensibilité ont é été faites avec une censure administrative réalisée à différentes échéances ([195] page 235).
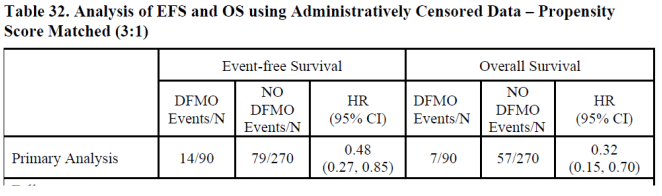
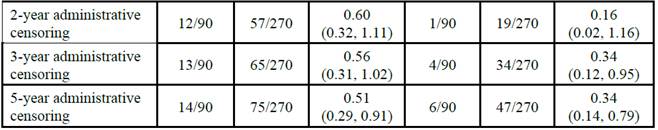
Pour les cas où le délai de suivi est fixe et identique pour tous les patients, l’émulation dans le groupe contrôle est simple. Se pose cependant le problème de l’irrégularité des temps de mesure du critère de jugement dans les données de vraie vie. La valeur la plus proche du délai voulu est alors utilisée si l’écart n’est pas trop grand (à fixer dans le protocole de l’étude). Cela entrainera une variabilité du temps de mesure pouvant avoir des conséquences en termes de pertinence clinique et des données manquantes sur le/les critères de jugement (si aucune mesure du critère de jugement proche du délai voulu n’est disponible).