2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
18 Identifications des patients dans la source de données
§ Cas particulier du groupe contrôle non traité
§ Captation des patients perdus de vue
18.2 Représentation graphique du processus d’extraction des données de l’étude
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
Il est important que la définition du suivi puisse faire apparaitre les patients perdus de vue. En effet, ces études utilisent souvent tout le suivi disponible pour un patient dans la source de données, c’est-à-dire jusqu’à l’événement critère de jugement ou la date de dernières nouvelles disponibles sans définir une date de fin de suivi théorique/attendu par patient. En procédant ainsi, les données paraissent parfaites (sans censures liées à des suivis interrompus précocement, donc sans perdus de vue) et contrastent avec les données du groupe traité où il peut exister de telles censures. Dans ce cas il ne sera pas possible de s’interroger sur la possibilité d’un biais d’attrition de fait de suivi censuré précocement et potentiellement informatif dans le groupe contrôle et qui existe en réalité.
Par exemple le patient est décédé à domicile ou dans un autre hôpital/service et le service/médecin assurant le remplissage du registre n’a pas eu l’information ou celle-ci n’a pas été saisie, car la saisie ne s’effectuant que l’on des consultations.
La sélection des patients sur la base de la disponibilité d’un suivi minimal expose à un biais de sélection, car l’inclusion/non inclusion dans le groupe contrôle pourra dépendre de la survenu du critère de jugement (cf. Figure 19). En effet un patient n’ayant pas le suivi minimal voulu peut être un patient perdu de vue rapidement après le début de son traitement. L’exclure conduira à méconnaitre le fait qu’il y a un patient perdu de vue pouvant conduire à sous-estimer la fréquence/taux de l’événement dans le groupe contrôle. L’inclure ne permettra pas de savoir s’il a fait l’événement ou pas (il est perdu de vue de toute façon) mais alertera sur le fait qu’il existe des patients perdus de vue pouvant biaiser le résultat de la comparaison. Le biais sera plutôt conservateur sauf si l’objectif et de ne pas mettre en évidence de différence (non-infériorité, safety).
Pour éviter cette problématique, les patients inclus dans le groupe contrôle doivent être identifiés uniquement sur le fait qu’ils vérifient les critères d’éligibilité dans une fenêtre temporelle prédéfinie et qui leur assure un suivi minimal compte tenu de la date de point retenue pour l’analyse (ou la date d’extraction des données de la source ou la date de dernière mise à jour de la source de données). Cette procédure (cf. Figure 19) permettra d’inclure des patients indépendamment de leur durée de suivi et inclura par exemple des patients dont le suivi s’est terminé prématurément avant la date de point retenue. Elle permet de recréer dans l’histoire passée des patients de la source de données le même processus d’inclusion et de suivi que dans une étude prospective monobras ou essai randomisé.
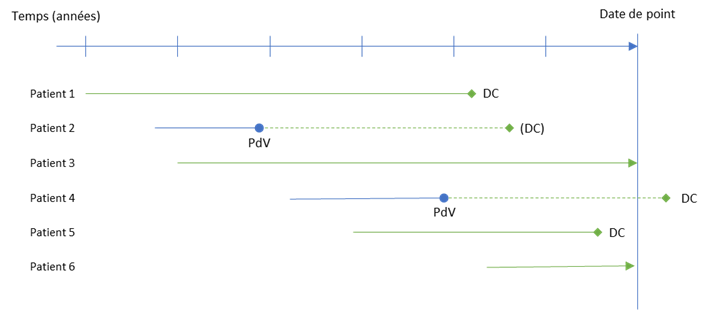
A |
B |
Figure 19 – Problèmes induits par une sélection des patients sur la durée de suivi et solution à adopter La sous-figure A illustre une sélection des patients qui ont au moins 2 ans de suivi (durée considérée comme nécessaire pour voir apparaitre les événements que le traitement cherche à éviter). Dans le jeu de données (figure du haut) il y a deux patients qui sont perdus de vue moins de 2 ans après le début de traitement. Ils ne sont donc pas sélectionnés et l’étude ne contient aucun perdu de vue, faisant croire à tort qu’elle est exempte de ce problème . Dans la sous-figure B, les patients n’ont pas été sélectionnés sur la durée effective de leur suivi disponible dans la source de données. Seuls ont été exclus les patients dont le traitement avait débuté moins de 2 ans avant la date de point (de ce fait ces patients ne pouvaient pas avoir la durée minimale de suivi permettant de voir apparaitre les événements). En revanche, les patients perdus de vue ont tous débuté leur traitement plus de deux ans avant la date de point. Ils sont donc inclus. Il apparait alors qu’il y a deux perdus de vue pouvant entrainer un biais.
Une fois la date de point fixée, il est possible de trouver la date de fin de la fenêtre d’inclusion qui est cette date moins la durée minimale de suivi que l’on souhaite avoir (par exemple la même que dans le groupe traité). Ensuite il est possible de remonter dans le temps jusqu’à ce que le nombre de patients éligibles soit trouvé.