2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
18 Identifications des patients dans la source de données
20.1.2 Origine des erreurs de classification
20.2 Complétudes, exhaustivité
20.3 Informativité, pertinence (relevance )
20.3.2 Critères d’éligibilité (de sélection des patients de la population visée)
20.5 La validation des données
20.6 Recommandations pour la constitution des sources de données
20.7 La rwPFS en oncologie
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
Un critère de jugement habituel dans les essais cliniques en oncologie est la survie sans progression (progression free survival , PFS ) qui mesure le temps jusqu’à la progression du cancer ou jusqu’au décès si celui survient sans progression préalable. La progression est mesurée à l’aide d’imageries répétées (comme un scanner tous les 3 mois, la périodicité dépendant de la pathologie étudiée) et avec l’utilisation de critère formel de progression, les critères RECIST.
Compte tenu de difficulté d’interprétation survenant parfois avec des clichés ambigus, ces mesures sont souvent effectuées, non pas par les investigateurs eux-mêmes, mais de façon centralisée par un comité d’adjudication, IRB.
Dans la pratique médicale courante, en dehors de la réalisation d’un essai clinique, les progressions sont diagnostiquées par les médecins traitants sans utiliser les critères RECIST, à partir d’imagerie réalisée en fonction des besoins cliniques et sans la stricte périodicité des protocoles des essais.
Il est donc impossible de mesurer la PFS dans des données de vraie vie.
Pour pallier cette impossibilité, il a été cherché des proxys évaluables avec les données disponibles dans les sources habituelles : dossiers médicaux, registres, etc. Ces proxys peuvent être le temps jusqu’à progression telle que notée dans les dossiers par les médecins traitants ou le temps jusqu’à l’arrêt du traitement ou à son changement pour un autre (le constat d’une progression du cancer conduit fréquemment à changer de ligne de traitement c’est-à-dire à utiliser un nouveau traitement). On rencontre ainsi à la place de la rwPFS le temps jusqu’au prochain traitement (rwTTNT real world time to next treatment ). Se pose aussi la question des changements de traitement sans progression identifiable. Se superpose aussi la question des censures qui suivent des règles très strictes dans les essais randomisés sans équivalent en observationnel (la notion de scanner manqué n’existe pas en observationnelle par exemple).
Compte tenu de ces différences fondamentales, la mesure effectuée sur les données observationnelles est classiquement appelée real world PFS, rwPFS afin de bien expliciter qu’il ne s’agit pas de la PFS.
Ainsi le terme rwPFS peut couvrir des réalités différentes en fonction de la source de données utilisée ou de la situation (en dernière ligne la progression ne se traduira pas par un changement de traitement, toutes les ressources thérapeutiques ayant été épuisées par exemple). Il est aussi possible de définir la rwPFS de très nombreuses façons [229] .
La rwPFS va différer de la PFS pour deux raisons (Figure 20) : les erreurs de classement liées à l’absence d’utilisation des critères RECIST et la non-périodicité des imageries [230] [231] . Plusieurs études ont montré que la rwPFS conduisait à une estimation biaisée de la PFS [231] [231] [26].
Les erreurs de classement conduisent à des faux positifs : à un temps donné, les données de RWD sont en faveur d’une progression (avis du clinicien ou du radiologue, changement de traitement, etc.) alors que si les critères RECIST avaient été appliqués la progression n’aurait pas (encore) été diagnostiquée ; mais aussi à des faux négatifs : dans la vraie vie, rien ne suggère une progression (pas de changement de traitement ou absence de mention de progression radiologique) alors que si les critères RECIST avaient été appliqués ils auraient conclu à une progression. Dans ces 2 cas, le temps jusqu’à événement mesuré avec la rwPFS sera différent de celui mesuré avec la PFS
L’irrégularité de la surveillance conduira aussi à des temps jusqu’à un événement différent avec la rwPFS et la PFS. Dans la vraie vie le scanner peut être effectué plus ou moins en fonction de la clinique, par exemple, quand celle-ci laisse fortement suspecter une progression (symptômes, altération de l’état général, etc.). Dans ce cas la progression sera détectée plus tardivement qu’avec une imagerie régulière qui aurait détecté la progression radiologique avec les signes cliniques. Mais il est aussi possible que l’imagerie guidée par la clinique soit effectuée un peu plus tôt que ce qu’elle aurait dû être dans le schéma de surveillance d’un essai clinique (dans ce contexte malgré les signes d’appels, la date programmée du scanner est attendue).
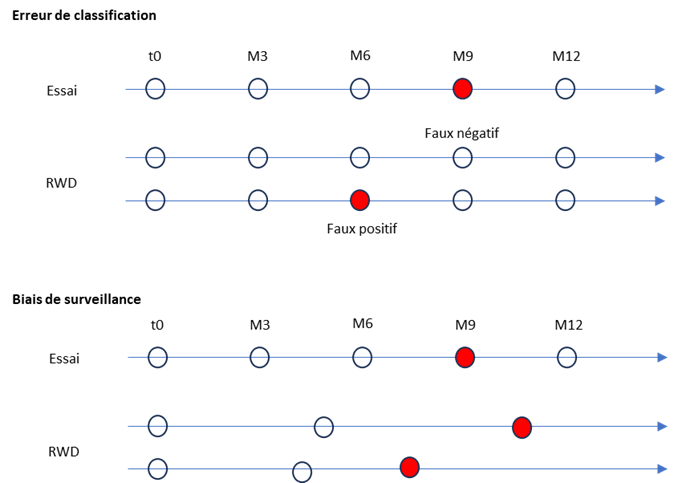
Figure 20 – Illustration des 2 biais affectant la rwPFS par rapport à la PFS La ligne temporelle « essai » représente ce qui se passe avec l’évaluation de la PFS ; les 2 autres lignes illustrent ce qui peut se passer avec une évaluation de la rwPFS à partir de données de vraie vie. Dans tout les cas, l’analyse portera sur le temps jusqu’à événement (du t0 au point rouge) qui peut donc être notablement différent entre PFS et rwPFS.
Si, dans une certaine mesure, ces biais peuvent ne pas trop perturber la comparaison de deux groupes utilisant la même définition du critère de jugement, ils auront bien plus de conséquences dans les comparaisons à un groupe contrôle externe. En effet dans ce cas la comparaison se fera entre la PFS dans le groupe traité et la rwPFS dans le groupe contrôle, soit entre deux concepts différents. Cette problématique ne peut pas être solutionnée en cherchant à mesurer aussi la rwPFS dans le groupe expérimental, car cela est impossible.
Au total, l’évaluation du bénéfice d’un nouveau traitement sur la PFS par une comparaison externe à un groupe contrôle externe issu de données observationnelles s’avère impossible. L’utilisation d’un groupe contrôle issu des données d’un essai clinique précédent utilisant la PFS usuelle est cependant envisageable.
L’évaluation du bénéfice du nouveau traitement sur la PFS à l’aide d’un groupe contrôle externe basé sur des données de vraie vie est très problématique et doit être évitée
Des méthodes d’analyse statistique permettant de comparer sans biais une PFS à la rwPFS ont été récemment proposées [232] [233] mais cette méthode repose sur des hypothèses fortes, en général invérifiables et sa réelle aptitude à corriger des biais va être très difficilement à établir de manière empirique, car rwPFS et PFS ne peuvent être mesuré simultanément sur les mêmes données. D’autres propositions sont en cours de développement note n° 24 .
En oncohématologie, les critères de progression sont souvent biologiques et peut-être plus facilement identifiables dans les bases de données contenant la biologie des patients.
Les limites de la rwPFS dans les comparaisons externes font que le critère de jugement d’élection pour les comparaisons externes en oncologie tumeurs solides doit être la survie globale (overall survival , OS). L’OS pose moins de problèmes métrologiques et de plus c’est le critère cliniquement pertinent par excellence.
Il faut cependant noter que l’information sur les décès n’est pas forcément complète dans beaucoup de sources de données. Les dossiers médicaux hospitaliers peuvent ne pas rapporter le décès et la date de décès d’un patient quand celui-ci est survenu à l’extérieur de l’établissement (comme au domicile ou dans un autre établissement). Il en est de même pour les registres qui sont remplis au fur et à mesure des consultations ou hospitalisations. On parle d’ailleurs parfois de rwOS (real world Overall Survival) pour alerter sur ce point.
Un chainage avec un registre d’état civil peut solutionner le point [234] [235] .
[24]https://www.ema.europa.eu/en/documents/presentation/presentation-quantifying-mitigating-measurement-bias-real-world-endpoints-when-constructing-external-control-arms-b-ackerman_en.pdf