2 TL ; DR - Guide d’évaluation des comparaisons à un groupe contrôle externe
3 Les études de comparaison externe, de quoi s’agit-il ?
5 Les problématiques méthodologiques soulevées par les comparaisons externes
6 Les comparaisons externes sont des études observationnelles
7 Position des agences de régulation et de HTA
8 De la nécessité d’avoir des preuves de l’intérêt cliniques des nouveaux traitements
9 Les sources de données utilisables
10 Les problématiques liées à l’aspect rétrospectif de ces études
12 Démarche hypothético déductive
13 L’inférence causale et les hypothèses sous-jacentes
15 Les techniques d’analyses statistiques
16 Le diagnostic d’absence de biais de confusion résiduel
18 Identifications des patients dans la source de données
21 Les outils d’évaluation du risque de biais
22 L’émulation d’un essai cible
22.1 Mise en œuvre
22.2 Évaluation des performances de l’approche
23 Le benchmarking et les contrôles positifs
24 Analyses de sensibilité , analyses quantitatives du biais
26 Contrôle du risque alpha global
En pratique l’émulation d’un essai cible consiste à élaborer le protocole (ou tout du moins son synopsis) de l’essai cible, puis à émuler par l’analyse des données observationnelle chaque élément méthodologique de cet essai, c’est-à-dire à construire une étude observationnelle qui mime ce qui se passerait si l’essai cible avait été réalisé [244] . Cette façon de procéder permet d’éviter des défauts de conception dans l’analyse des données observationnelles en particulier au niveau du biais de sélection biais par temps d’immortalité ou lié à un objectif ne se traduisant pas par une question causale.
Les éléments constitutifs de l’essai cible qui sont à émuler sont les suivants :
Un point sensible dans l’émulation est la détermination du t0 de début de suivi qui conditionne la protection contre le biais de sélection des études [197] . Cette problématique est détaillée section 18.1.1.
En pratique cette démarche débouche sur un tableau présentant les éléments de l’essai cible et la façon dont ces éléments seront émulés dans l’étude observationnelle.
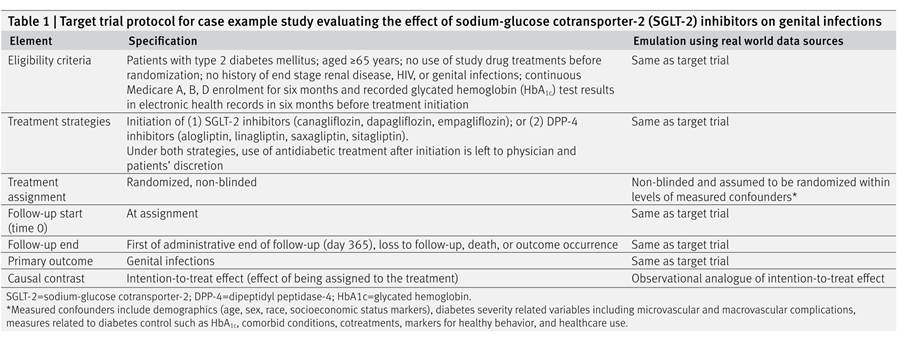
Figure 21 - Exemple de tableau décrivant l’émulation d’un essai cible (extrait de [87] )
Un guide de rédaction EQUATOR note n° 26 spécifique, dénommé TARGET, liste les informations indispensables à rapporter dans une publication (ou un rapport) d’une étude basée sur une émulation d’essais cible [245] .
L’émulation de l’essai de cible est mentionnée dans plusieurs guidelines comme celui de la FDA sur les études observationnelles (non-interventionnelles) [48] ou le position paper de l’HAS [44] .
Agence |
Document |
Page |
Extrait |
EMA |
Reflection paper on use of real-world data in noninterventional studies to generate real-world evidence for regulatory purposes |
7 |
The target trial emulation (TTE) framework should be considered as a strategy that uses existing tools and methods to formalise the design and analysis of NIS using RWD with causal objectives |
MHRA |
MHRA draft guideline on the use of external control arms based on real- world data to support regulatory decisions |
NA |
NA |
MHRA |
MHRA guidance on the use of real-world data in clinical studies to support regulatory decisions |
NA |
NA |
FDA |
Real-World Evidence: Considerations Regarding Non-Interventional Studies for Drug and Biological Products [53] |
5 |
Several conceptual approaches can be used to address concerns regarding causality when designing a noninterventional study, including, but not limited to, the emulation of a hypothetical clinical trial that addresses the research question of interest. |
FDA |
Considerations for the Design and Conduct of Externally Controlled Trials for Drug and Biological Products [6] |
NA |
NA |
HAS |
Rapid access to innovative medicinal products while ensuring relevant health technology assessment. Position of the French National Authority for Health [44] |
||
NICE |
NICE real-world evidence framework [64] |
[26] https://www.equator-network.org/reporting-guidelines/