#FL012 Traitement du carcinome bronchique à petites cellules par le tarlatamab
Contexte
Le carcinome bronchique à petites cellules (CBPC) représente 15% des tumeurs bronchiques primitives(1,2), il s’agit d’un cancer de mauvais pronostic avec une survie à 5 ans < 5% en cas de cancer localement avancé ou métastatique(3).
Le traitement des CBPC localement avancé et métastatique repose en 1ère ligne sur une polychimiothérapie par sels de platine et étoposide associée à une immunothérapie anti-PDL1(4,5). Le CBPC est initialement chimio-sensible avec un taux de réponse objectif de 60-70%(4,5), cependant la majorité des patients rechutent après les traitements de 1ère ligne(6–8). A la progression, le traitement de 2ème ligne repose sur des chimiothérapie (rechallenge des sels de platine, topotecan, polychimiothérapie ou lurbinectidine), avec une survie globale en 2ème ligne de 7-9 mois(9–12).
Mécanisme d’action
Le tarlatamab est un anticorps bispécifique ciblant les lymphocytes T CD3 (LTCD3) et le delta-like ligand 3 (DLL3) exprimé sur 85-96% des cellules tumorales des CBPC(13–16).
Etude DeLLphi-304
L’étude de phase 3 Tarlatamab in Small-Cell Lung Cancer after Platinum-Based Chemotherapy(17), dont les résultats de l’analyse intermédiaire ont été publiée dans le New England Journal of Medicine en juin 2025, évalue l’efficacité et la sécurité du tarlatamab dans le traitement de 2ème ligne des patients atteints d’un CBPC.
|
Critères PICO |
|
|
Patients |
CBPC en progression en cours ou après un traitement de 1ère ligne par platine |
|
Intervention |
Tarlatamab |
|
Comparateur |
Chimiothérapie (topotecan, lurbinectidine, amrubicine) |
|
Outcomes |
Survie globale (critère de jugement principal) |
|
Study desing |
Essai contrôlé, randomisé, de supériorité, en ouvert, multicentrique |
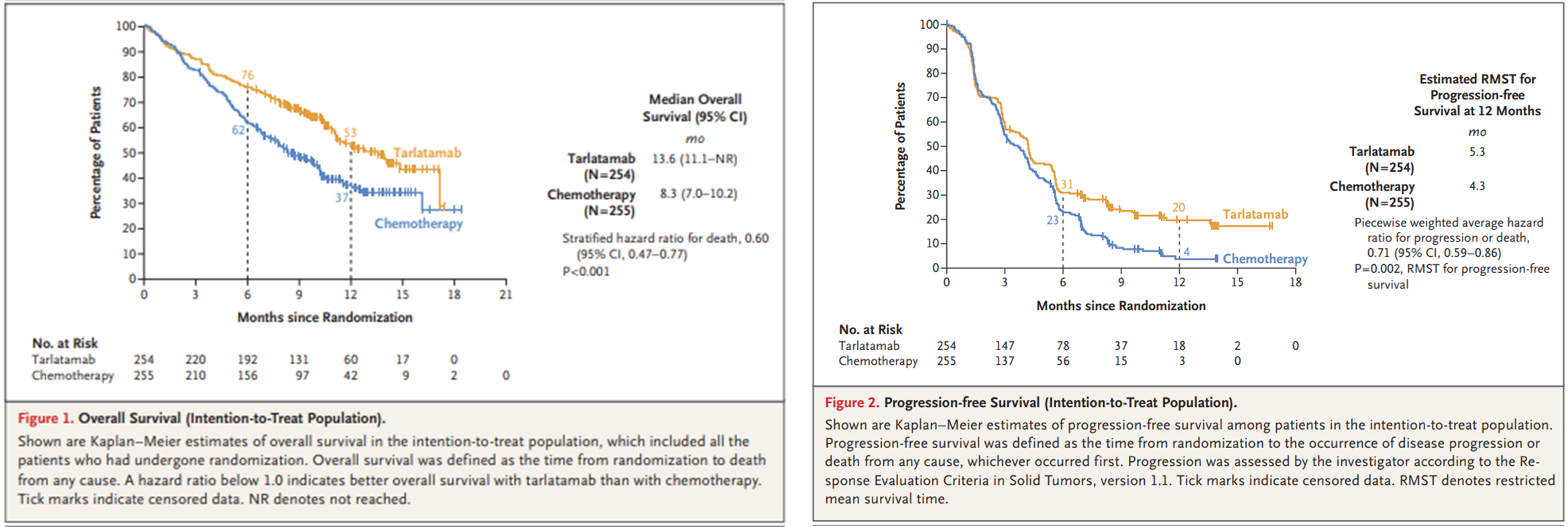
Après un suivi médian d’environ 11 mois, les patients du groupe tarlatamab ont une réduction du risque de décès de 40% par rapport à ceux traités par chimiothérapie standard (Figure 1, HR 0.60 [95% 0.47 – 0.77]. L’étude a également montré une différence significative sur le taux de réponse objectif (35% dans le groupe tarlatamab et 20% dans le groupe chimiothérapie). La survie sans progression médiane était comparable entre les groupes (4,2 mois pour le tarlatamab contre 3,7 mois pour la chimiothérapie). En raison de la non-validité de l’hypothèse des risques proportionnels, une analyse de la survie sans progression par temps de survie moyen restreint (RMST) à 12 mois a été réalisée, montrant une différence significative en faveur du tarlatamab (Figure 2, HR 0.71 [95 0.59 – 0.86]).
Concernant le profil de sécurité, la toxicité du tarlatamab semble acceptable comparativement au traitement standard par chimiothérapie. Dans l’étude, il y avait moins d’effets indésirables grade ³ 3 dans le groupe tarlatamab (54%) que dans le groupe chimiothérapie (80%). Les effets indésirables de grade ³ 3 les plus fréquents avec le tarlatamab étaient les cytopénies, l’asthénie et l’hyponatrémie. Un syndrome de relargage cytokinique (CRS) était survenu chez 56% des patients traités par tarlatamab parmi lesquelles 42% de CRS de grade 1, 13% de grade 2, 1% de grade 3 et aucun CRS de grade 4 ou 5.
Au total, le tarlatamab est une nouvelle option thérapeutique dans le traitement des patients avec un CBPC localement avancé ou métastatique, avec un gain significatif en survie globale pour des patients chez lesquelles les options thérapeutiques étaient jusqu’alors limitées. Le tarlatamab a été approuvé par la FDA en mai 2024 comme traitement de 2ème ligne des CBPC(18), il n’a actuellement pas d’AMM dans l’union européenne.
- Wang S, Tang J, Sun T, Zheng X, Li J, Sun H, et al. Survival changes in patients with small cell lung cancer and disparities between different sexes, socioeconomic statuses and ages. Sci Rep. 2 mai 2017;7(1):1339.
- Oronsky B, Reid TR, Oronsky A, Carter CA. What’s New in SCLC? A Review. Neoplasia. oct 2017;19(10):842‑7.
- Bethesda, MD. Surveillance Research Program. SEER*Explorer: an interactive website for SEER cancer statistic [Internet]. 2024 [cité 6 juill 2025]. Disponible sur: https://seer.cancer.gov/statistics -network/explorer/
- Horn L, Mansfield AS, Szczęsna A, Havel L, Krzakowski M, Hochmair MJ, et al. First-Line Atezolizumab plus Chemotherapy in Extensive-Stage Small-Cell Lung Cancer. New England Journal of Medicine. 6 déc 2018;379(23):2220‑9.
- Paz-Ares L, Dvorkin M, Chen Y, Reinmuth N, Hotta K, Trukhin D, et al. Durvalumab plus platinum–etoposide versus platinum–etoposide in first-line treatment of extensive-stage small-cell lung cancer (CASPIAN): a randomised, controlled, open-label, phase 3 trial. The Lancet. 23 nov 2019;394(10212):1929‑39.
- Pietanza MC, Byers LA, Minna JD, Rudin CM. Small cell lung cancer: will recent progress lead to improved outcomes? Clin Cancer Res. 15 mai 2015;21(10):2244‑55.
- Farago AF, Keane FK. Current standards for clinical management of small cell lung cancer. Transl Lung Cancer Res. févr 2018;7(1):69‑79.
- Rossi A, Di Maio M, Chiodini P, Rudd RM, Okamoto H, Skarlos DV, et al. Carboplatin- or cisplatin-based chemotherapy in first-line treatment of small-cell lung cancer: the COCIS meta-analysis of individual patient data. J Clin Oncol. 10 mai 2012;30(14):1692‑8.
- von Pawel J, Jotte R, Spigel DR, O’Brien MER, Socinski MA, Mezger J, et al. Randomized phase III trial of amrubicin versus topotecan as second-line treatment for patients with small-cell lung cancer. J Clin Oncol. 10 déc 2014;32(35):4012‑9.
- Trigo J, Subbiah V, Besse B, Moreno V, López R, Sala MA, et al. Lurbinectedin as second-line treatment for patients with small-cell lung cancer: a single-arm, open-label, phase 2 basket trial. Lancet Oncol. mai 2020;21(5):645‑54.
- Horita N, Yamamoto M, Sato T, Tsukahara T, Nagakura H, Tashiro K, et al. Topotecan for Relapsed Small-cell Lung Cancer: Systematic Review and Meta-Analysis of 1347 Patients. Sci Rep. 21 oct 2015;5:15437.
- Onoda S, Masuda N, Seto T, Eguchi K, Takiguchi Y, Isobe H, et al. Phase II trial of amrubicin for treatment of refractory or relapsed small-cell lung cancer: Thoracic Oncology Research Group Study 0301. J Clin Oncol. 1 déc 2006;24(34):5448‑53.
- Giffin MJ, Cooke K, Lobenhofer EK, Estrada J, Zhan J, Deegen P, et al. AMG 757, a Half-Life Extended, DLL3-Targeted Bispecific T-Cell Engager, Shows High Potency and Sensitivity in Preclinical Models of Small-Cell Lung Cancer. Clin Cancer Res. 1 mars 2021;27(5):1526‑37.
- Rojo F, Corassa M, Mavroudis D, Öz AB, Biesma B, Brcic L, et al. International real-world study of DLL3 expression in patients with small cell lung cancer. Lung Cancer. sept 2020;147:237‑43.
- Paz-Ares L, Champiat S, Lai WV, Izumi H, Govindan R, Boyer M, et al. Tarlatamab, a First-in-Class DLL3-Targeted Bispecific T-Cell Engager, in Recurrent Small-Cell Lung Cancer: An Open-Label, Phase I Study. J Clin Oncol. 1 juin 2023;41(16):2893‑903.
- Ahn MJ, Cho BC, Felip E, Korantzis I, Ohashi K, Majem M, et al. Tarlatamab for Patients with Previously Treated Small-Cell Lung Cancer. N Engl J Med. 30 nov 2023;389(22):2063‑75.
- Mountzios G, Sun L, Cho BC, Demirci U, Baka S, Gümüş M, et al. Tarlatamab in Small-Cell Lung Cancer after Platinum-Based Chemotherapy. New England Journal of Medicine [Internet]. [cité 16 juin 2025];0(0). Disponible sur: https://www.nejm.org/doi/full/10.1056/NEJMoa2502099
- Research C for DE and. FDA grants accelerated approval to tarlatamab-dlle for extensive stage small cell lung cancer. FDA [Internet]. 16 mai 2024 [cité 6 juill 2025]; Disponible sur: https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-tarlatamab-dlle-extensive-stage-small-cell-lung-cancer
- Dernière mise à jour le .
